| Tema | Nomenclatura, Reacciones , Síntesis y Obtención de Hidrocarburos Alifáticos |
|---|---|
| Evidencia | |
| calificable? | 0 |
| Activo | 1 |
Propósito
Explica los principios de la nomenclatura síntesis y obtención de hidrocarburos y deduce su importancia mediante la resolución de guía de trabajo alusiva al tema para tener herramientas reflexivas frente al uso de combustibles fósiles y su impacto en el medio ambiente.
Motivación
07.04.2021 - American Chemical Society (ACS)
¿Biocombustibles de la fábrica de cerveza?
Separación de los residuos de cerveza en proteínas para alimentos y fibra para biocombustibles
Explicación
Los hidrocarburos alifáticos son los compuestos orgánicos no derivados del benceno. Están formados por átomos de carbono e hidrógeno, formando cadenas, las cuales pueden ser abiertas o cerradas.
Los hidrocarburos pueden encontrarse unidos por enlaces simples, dobles o triples. Como el carbono es tretavalente, está compartiendo dos electrones en cada enlace, y el hidrógeno, que solamente tiene un electrón, sólo necesita un enlace para poder juntarse con el carbono.
Los hidrocarburos alifáticos son ampliamente utilizados como disolventes, pues pueden disolver sustancias aceitosas, grasas, resinas o incluso caucho y otras sustancias, hecho muy útil en la industria de obtención de sustancias como pinturas, pegamentos, y un largo etc., así como también son de gran utilidad en la síntesis en química orgánica, donde son a menudo utilizados como materia prima.
Dentro del grupo de hidrocarburos alifáticos de cadena abierta tenemos a los alcanos, alquenos y alquinos, diferentes en base a la naturaleza de sus enlaces, y dentro del grupo de hidrocarburos de cadena cerrada, tendremos a aquellos compuestos que se cierran su cadena formando un anillo sin ser derivados del benceno, como por ejemplo, los cicloalcanos.
Los hidrocarburos alifáticos pueden ser “no saturados”, en los casos de las cadenas unidas con dobles o triples enlaces, o saturados, cuando todos los enlaces que conforman la molécula son de tipo simple.
Los hidrocarburos alifáticos se subdividen en: alcanos, alquenos y alquinos.
- Alcanos: Son hidrocarburos alifáticos, también conocidos como de cadena abierta, constituidos por carbonos e hidrógenos unidos por enlaces sencillos.
Responden a la fórmula CnH2n+2, de donde n es el número de carbonos. Para nominar a este tipo de hidrocarburos, se debe ver el número de carbonos que posea la cadena, de manera que podamos anteponer el prefijo griego (met, et, prop, but, etc), añadiendo la terminación –ano.
Los primeros de la serie son:
Metano: CH4
Etano: CH3-CH3
Propano: CH3-CH2-CH3
Butano: CH3-CH2-CH2-CH3
Los hidrocarburos alifáticos saturados, siguen la fórmula de tipo CnH2n+2, de donde n hace referencia al número de átomos de carbono. Estos compuestos que poseen el mismo grupo funcional (el enlace), pero tienen diferente número de átomos, forman lo que se conoce como serie homóloga.
Los hidrocarburos alifáticos pueden ser “no saturados”, en los casos de las cadenas unidas con dobles o triples enlaces, o saturados, cuando todos los enlaces que conforman la molécula son de tipo simple.
Los hidrocarburos alifáticos se subdividen en: alcanos, alquenos y alquinos.
- Hidrocarburos Saturados Alcanos: Son hidrocarburos alifáticos, también conocidos como de cadena abierta, constituidos por carbonos e hidrógenos unidos por enlaces sencillos. Responden a la fórmula CnH2n+2, de donde n es el número de carbonos. presentan enlaces sencillos entre sus átomos de carbono. (Enlaces sigma).
Cual seria la formula molecular para un hidrocarburo cuando n= 3
C3 H2*3 + 2 = C3H8 H3C - CH2 – CH3 PROPANO
Los alcanos utilizan el sufijo ANO para indicar que los enlaces entre los átomos de carbono son sencillos.
Se llaman también parafinas, son poco reactivos debido a los enlaces sencillos (saturados)
CARACTERISTICAS FISICAS • Las propiedades físicas cambian en función del peso molecular.
• El punto de ebullición sube en función del peso molecular, hasta C4 aparecen como gases.
• Los puntos de ebullición de los hidrocarburos ramificados son menores que los de los hidrocarburos lineales, a igual número de carbonos.
• Respecto al punto de fusión las moléculas redondeadas se empaquetan mejor que las lineales y tienen mayores puntos de fusión.
Prefijos que se utilizan para indicar la cantidad de carbonos de la cadena principal:
Met: 1 carbono
Et : 2 carbonos
Prop: 3 carbonos
But: 4 carbonos
Pent: 5 carbonos
Hex: 6 carbonos
Hept: 7 Carbonos
Oct: 8 Carbonos
Non: 9 Carbonos
Dec: 10 Carbonos
Undec: 12 Carbonos
Estados de Agregación de los alcanos:
Cuando el máximo de carbonos es : gaseosos ( metano, etano, propano, butano, pentano)
Desde 6 carbonos hasta 12 carbonos: se encuentran en estado líquido.
1. encontrar la cadena carbonada más larga, debe ser continua. Señalar esta cadena.
2. identificar las ramificaciones.
3. determinar por cual extremo se debe numerar la cadena( por el extremo donde esté más cerca la primera ramificación).
4. nombrar las ramificaciones en “ORDEN ALFABÉTICO”
5. Las ramificaciones iguales se ubican mencionando el carbono donde se ubica esta ramificación (si en el mismo carbono hay dos ramificaciones iguales se debe mencionar dos veces el número del carbono donde se encuentren estas ramificaciones) , de ser necesario se utilizaran los prefijos :
Di: si la ramificación se repite 2 veces
Tri: si la ramificación se repite 3 veces
Tetra: si la ramificación se repite 4 veces
6. indicar el prefijo que indica cantidad de carbonos de la cadena mas larga y utilizar el sufijo ANO.
Ejemplo:
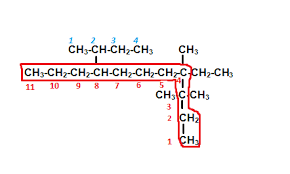
otro ejemplo de selección de cadena mas larga e identificación de sustituyentes
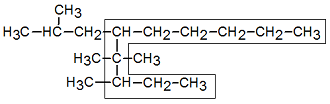
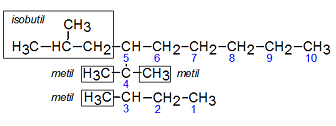
Para el siguiente hidrocarburo se puede observar la seleccion de la cadena más larga y los radicales o sustituyentes. el nombre para este hidrocarburo sera:
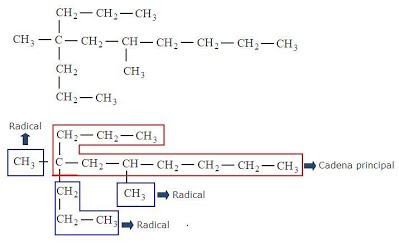
observe los siguientes videos para ayudarse en el proceso
https://www.youtube.com/watch?v=3TmTDYyQBjo
https://www.youtube.com/watch?v=IH5duXi1xis
REACCIONES DE LOS ALCANOS: Las reacciones más importantes de los alcanos son la pirólisis,la combustión y la halogenación.
1. Pirolisis:

2.

3. Halogenacion: esta es una reacción de sustitución. en la ecuación general X2 es el halógeno ( Cloro, bromo o yodo) R-H: cadena carbonada
X2 : halógeno ( F2, Cl2, Br2, I2)
HX: acido hidrácido( HF, HCl. HBr, HI)
R-X : halogenuro de alquilo
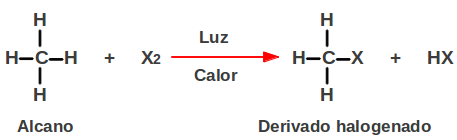
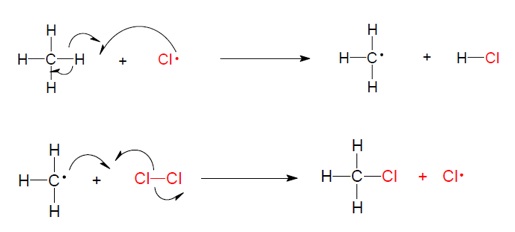
el anterior es el mecanismo de sustitución del hidrogeno del alcano por uno de los átomos de cloro.
se pueden realizar múltiples halogenaciones para obtener alcanos mono halogenados, di halogenados, trihalogenados o tetrahalogenados.
SISNTESIS DE ALCANOS: proceso de obtención de un alcano a partir de otro compuesto.
1. Síntesis de Grignard: se lleva a cabo en 2 etapas:
1. etapa: obtención del reactivo de grignard a partir de la adición de Mg metálico a un halogenuro de alquilo en presencia de éter
Éter seco
CH3Br + Mg --------------------CH3-MgBr(reactivo de Grignard) Bromuro de metil magnesio
2. etapa hidratación del reactivo de Grignard:
Obtener propano a partir de cloro propano:
Eter
CH3 – CH2- CH2MgCl + H2O --------- CH3-CH2-CH3 + Mg(OH)Cl
2. Síntesis de Wurtz: permite ampliar la cadena. Este método de obtención de alcanos se debe a Adolfo Wurtz.
La reacción general:
R – X + 2Na + X- R--------------R- R+Na X+ Na X
EJM: obtener butano a partir de bromo etano
CH3-CH2-Br+ 2Na + BrCH2-CH3 ------------- CH3-CH2-CH2-CH3+ 2 NaBr
3. Hidrogenación de alquenos. No hay aumento aumento de cadena carbonada. Se parte de un alqueno ( hay doble enlace en la cadena)el objetivo de la hidrogenación es eliminar el doble enlace para forma un alcano.
Pd /Ni
R=R+ H2-------------------- R -R
El paladio y Níquel son los catalizadores que permiten que la reacción se lleve a cabo.
Pd/ Ni
CH2 = CH2- CH3 + H2 ------------ CH3-CH2-CH3
Ejercicios
Escribir las fórmulas para los siguientes hidrocarburos:
1. 5,5 dietil- 2metil-4propil-decano
2. 4- isopropil- 3,3 dimetil-undecano
3. 4-etil- 5-isopropil- 3,4,7-trimetil-nonano4. Aignar nombre para cada uno de los siguientes hidrocarburos de acuerdo con las normas de nomenclatura:
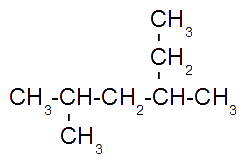
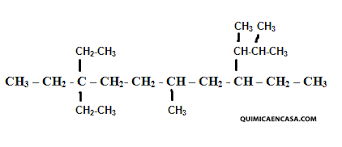
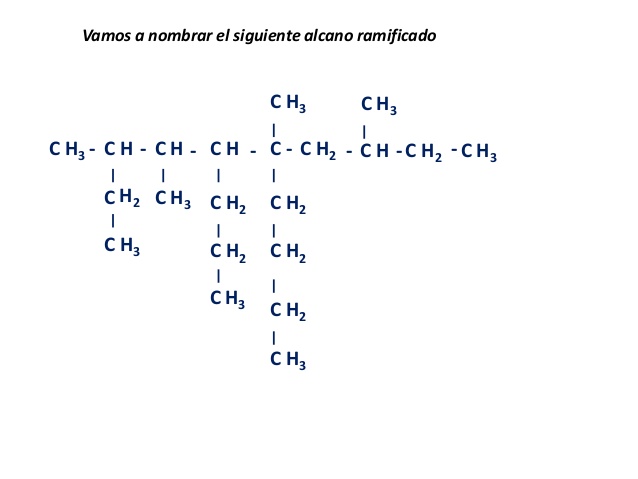
para los siguientes alcanos complete las reacciones:
1. 5,5 dietil- 2metil-4propil-decano + Cl2 ---------------
2. 4- isopropil- 3,3 dimetil-undecano + Br2 ------------
3. 4-etil- 5-isopropil- 3,4,7-trimetil-nonano + Cl2 ----------
Obtener
1. pentano a partir de bromo pentano
2. Butano a partir de cloro butano
Obtener
1. hexano a partir de cloro propano
2. octano a partir de bromo butano
3. metano a partir de cloro metano
Evaluación
Enlace quizz
Bibliografía
Foro
Cursos
| Curso | |
|---|---|
No results found. | |
Acceso a las actividades
| Actividad | Nombre | Fecha de ingreso | Fecha de actualización | Número de ingresos | Año | Curso | Subreporte |
|---|---|---|---|---|---|---|---|
No results found. | |||||||
