| Tema | Nomenclatura, Reacciones , Síntesis y Obtención de Hidrocarburos Alifáticos |
|---|---|
| Evidencia | |
| calificable? | 1 |
| Activo | 0 |
Propósito
Explica los principios de la nomenclatura de hidrocarburos y deduce su importancia mediante la resolución de guía de trabajo alusiva al tema para tener herramientas reflexivas frente al uso de combustibles fósiles y su impacto en el medio ambiente.
Motivación
Explicación
HIDROCARBUROS INSATURADOS ALQUENOS NOMENCLATURA- REACCIONES Y SÍNTESIS
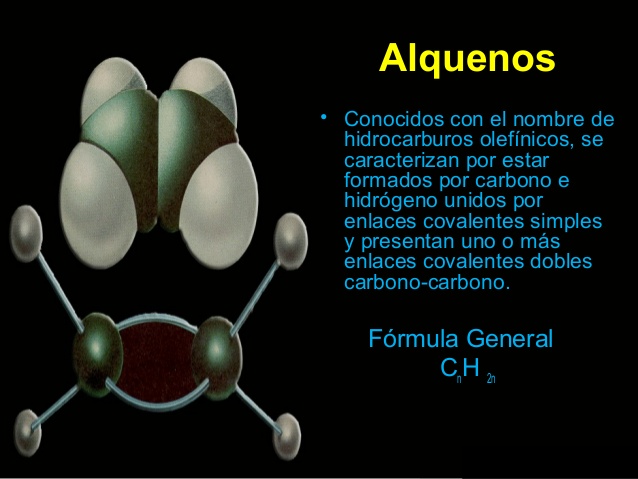
Los alquenos son hidrocarburos insaturados que tienen doble enlace carbono-carbono en su molécula.Su fórmula general es CnH2n Se puede decir que un alqueno es un alcano que ha perdido dos átomos de hidrógeno produciendo como resultado un enlace doble entre dos carbonos. Los alquenos cíclicos reciben el nombre de cicloalquenos.Se emplea frecuentemente la palabra olefina como sinónimo.
Los alquenos abundan en la naturaleza. El eteno, es un compuesto que controla el crecimiento de las plantas, la germinación de las semillas y la maduración de los frutos. CH2=CH2
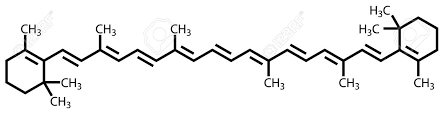
El ??Pineno es una fragancia obtenida a partir de los pinos.
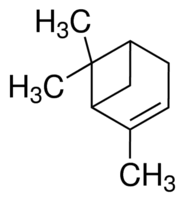
?-Caroteno es un compuesto que contiene 11 dobles enlaces y es precursor de la vitamina A.
 las zanahorias son una fuente de carotenos.
las zanahorias son una fuente de carotenos.
NOMENCLATURA DE ALQUENOS
Los alquenos se nombran reemplazando la terminación -ano del correspondiente alcano por -eno. Los alquenos más simples son el eteno y el propeno, también llamados etileno y propileno a nivel industrial.
Regla 1.- Se elige como cadena principal la de mayor longitud que contenga el doble enlace. La numeración comienza en el extremo que otorga al doble enlace el menor localizador.

Regla 2.- El nombre de los sustituyentes precede al de la cadena principal y se acompaña de un localizador que indica su posición en la molécula. La molécula se numera de modo que el doble enlace tome el localizador más bajo.
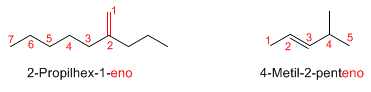
Regla 3.- Cuando hay varios sustituyentes se ordenan alfabéticamente y se acompañan de sus respectivos localizadores

Regla 4.- Cuando el doble enlace está a la misma distancia de ambos extremos, se numera para que los sustituyentes tomen los menores localizadores.

Regla 5.- En compuestos cíclicos resulta innecesario indicar la posición del doble enlace, puesto que siempre se encuentra entre las posiciones 1 y 2.
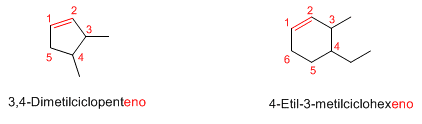
Algunos ejemplos:
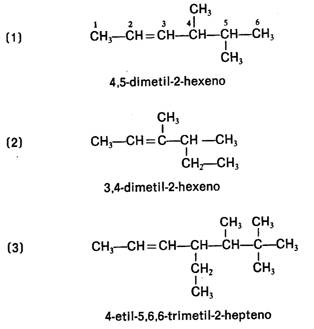
GRADO DE INSATURACION:
Cada anillo o ciclo de una molécula implica la pérdida de dos hidrógenos respecto a un alcano de fórmula CnH2n+2. Se denomina grado de insaturación al número de ciclos y dobles enlaces presentes en una molécula.. Debido a que los alcanos contienen el máximo número posible de enlaces carbono-hidrógeno, se dice de ellos que son hidrocarburos saturados. Alquenos y compuestos cíclicos son hidrocarburos insaturados.
CH3-CH2-CH2-CH3 El buteno: CH3-CH=CH-CH3
El número total de enlaces ? y ciclos en una molécula se denomina grado de insaturación
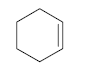
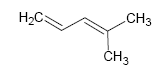
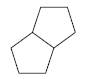
Grado de insaturación en compuestos que continenen halógenos, oxígenos y nitrógenos:
Halógenos: Sumar el número de halógenos al número de hidrógenos.
Oxígenos: Ignorar los oxígenos.
Nitrógenos: Restar el número de nitrógenos del número de hidrógenos.
{doc}Ejemplo 1: Calcular el grado de insaturación en las siguientes fórmulas:
a) C4H8
Solución: Un alcano saturado de 4 carbonos tiene de fórmula C4H10. El compuesto tiene un par de hidrógenos menos, así que, su grado de insaturación es uno.
b) C9H16Br2
Solución: Sumamos los halógenos a los hidrógenos obteniéndose la fórmula C9H18. Un alcano saturado de 9 carbonos tiene de fórmula C9H20. El compuesto tiene una insaturación.
ESTRUCTURA Y ENLACE
Los siguientes modelos muestran la estructura, distancias y ángulos de enlace del eteno. Cada uno de los carbonos de la molécula tiene hibridación sp2. Su geometría es plana, con ángulos de enlace próximos a los 120º.
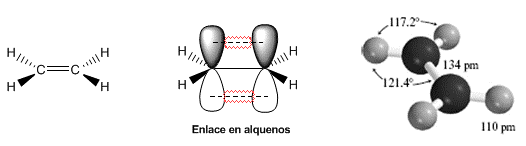
El doble enlace está formado por un enlace s que se obtiene por solapamiento de los orbitales híbridos sp2, y un enlace formado por solapamiento de orbitales p que no hibridaron (orbitales p puros).
El doble enlace es más fuerte y corto que el simple. La energía del doble enlace en el eteno es de 605 KJ/mol frente a los 368 KJ/mol del enlace simple carbono-carbono en el etano.
PROPIEDADES FISICAS DE LOS ALQUENOS
Los alquenos presentan puntos de fusión y ebullición próximos a los alcanos correspondientes.
CH2=CH2 P eb = -103°C
CH3-CH=CH2 P eb = -47 °C
Momento dipolar en alquenos.
El carbono sp2 tiene más carácter s que el carbono sp3, los electrones en el orbital s están más próximos al núcleo y son atraídos fuertemente por éste, de modo que un carbono sp2 tiene tendencia a atraer hacia si electrones, lo que genera momentos dipolares.
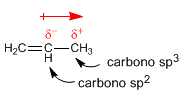
En alquenos trans los momentos dipolares se restan, llegando a anularse en el caso de que ambos carbonos tengan cadenas iguales. En los alquenos cis los momentos dipolares se suman dando lugar a un momento dipolar total distinto de cero (molécula polar)
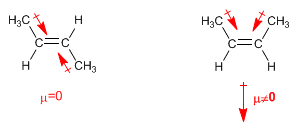
ESTABILIDAD DE LOS ALQUENOS
Los calores desprendidos en las siguientes reacciones de hidrogenación, nos dan una idea sobre la diferente estabilidad de los alquenos.
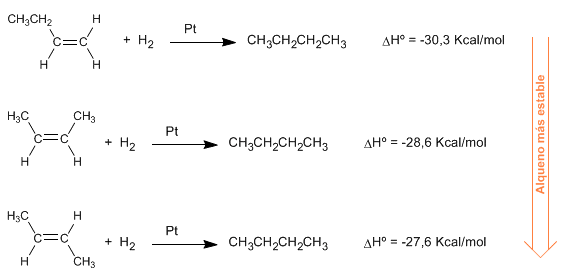
Los tres alquenos hidrogenan para dar el mismo alcano (butano). El 1-buteno es el alqueno que más energía desprende en la hidrogenación, por ello, es el más inestable (tiene más energía). Los cis y trans-1-buteno tienen una mayor estabilidad por ser alquenos más sustituidos. La interacción entre las cadenas que rodean el alqueno y el doble enlace (hiperconjugación) lo estabiliza, disminuyendo su energía.
Como puede observarse el cis-2-buteno es mas inestable que el trans, debido a las repulsiones estéricas entre metilos.
El orden de estabilidad de los alquenos es el siguiente:
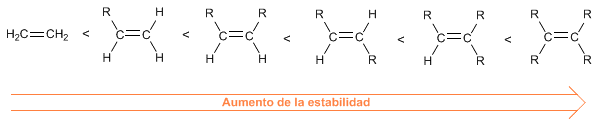
SINTESIS DE ALQUENOS MEDIANTE E2 (ELIMINACIÓN BIMOLECULAR)
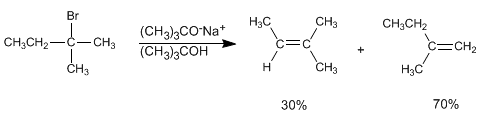
Los alquenos pueden prepararse a partir de haloalcanos y sulfonatos de alquilo mediante eliminación bimolecular (E2). En el siguiente ejemplo el 2-bromo-2-metilbutano reacciona con metóxido de sodio para formar una mezcla de 2-metil-2-buteno y 2-metil-1-buteno.
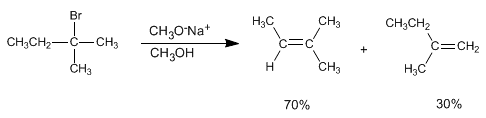
En esta eliminación se obtiene mayoritariamente el producto de mayor estabilidad (alqueno más sustituido), y se dice que sigue la regla de Saytzev.
El metóxido, base pequeña, sustrae el hidrógeno más interno del haloalcano para generar el producto más estable (alqueno termodinámico
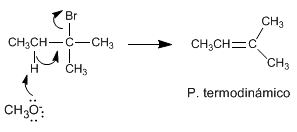
Si empleamos como base tert-butóxido o LDA el alqueno formado mayoritariamente es el 2-metil-1-buteno. Las bases impedidas tienen dificultades para acceder al hidrógeno más interno, sustrayendo más rápido el hidrógeno más accesible, por lo que generan el producto menos estable mayoritariamente. En este caso la reacción se controla cinéticamente y se de que sigue la regla de Hofmann.
Los hidrógenos situados sobre metilos son más accesibles para el tert-butóxido que los internos. El alqueno formado mayoritariamente es el menos sustituido.
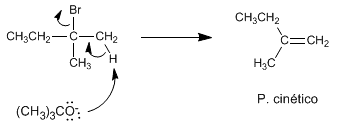
SINTESIS DE ALQUENOS POR DESHIDRATACION DE ALCOHOLES
El tratamiento de alcoholes con ácidos minerales a elevadas temperaturas provoca la pérdida e agua, que transcurre a través de mecanismos E1 o E2.
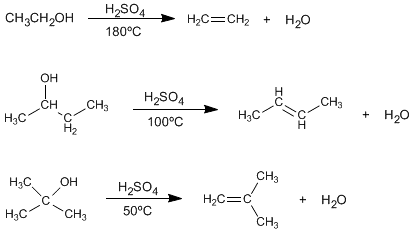
En las condiciones de reacción, se observa que los alcoholes terciarios deshidratan mejor que los secundarios, y estos a su vez mejor que los primarios.
Mecanismo para la deshidratación de alcoholes primarios
Los alcoholes primarios deshidratan mediante mecanismo E2
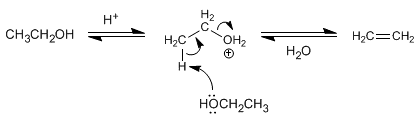
Mecanismo de la deshidratación de alcoholes secundarios o terciarios
Los alcoholes secundarios y terciarios forman carbocationes estables por pérdida de una molécula de agua previa protonación del grupo hidroxilo. El carbocatión formado genera el alqueno por pérdida de un protón.
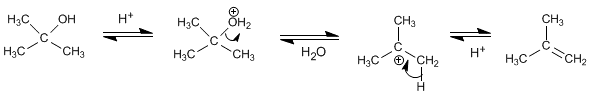
observe los siguientes videos para reafirmar sus conocimientos
https://www.youtube.com/watch?v=VdQSI_hyjQ8
https://www.youtube.com/watch?v=iQRtGLDAeoY
Ejercicios
Nombre los siguientes alcanos de acuerdo a las reglas vistas
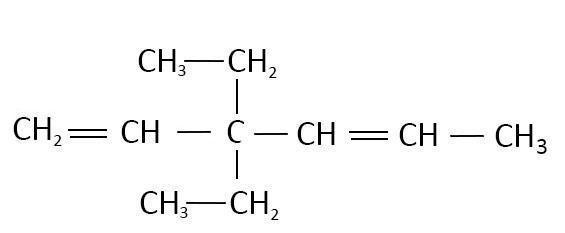
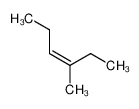
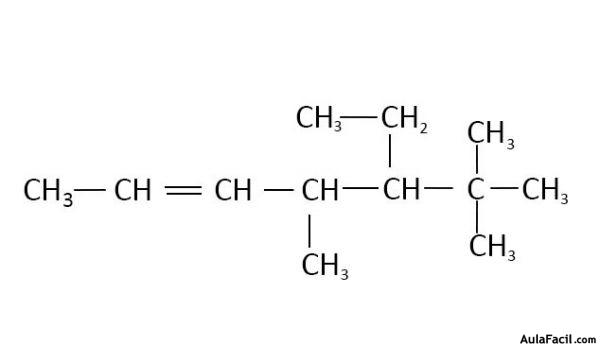
2. Calcular el grado de instauración para:
a.
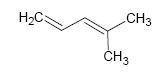
b. CH3-CH=CH-CH2Br
c. C8H16
3. Obtenga los siguientes alquenos
a. buteno a partir de butanol
b. eteno a partir de etanol
c. penteno a partir de 2 pentanol
d. propeno a partir de 2 bromo propano
e. hexeno a partir de 3 cloro hexano
Evaluación
enlace quizz
Bibliografía
Foro
Cursos
| Curso | |
|---|---|
No results found. | |
Acceso a las actividades
| Actividad | Nombre | Fecha de ingreso | Fecha de actualización | Número de ingresos | Año | Curso | Subreporte |
|---|---|---|---|---|---|---|---|
No results found. | |||||||