| Tema | tabla periódica |
|---|---|
| Evidencia | Fotografías de las actividades propuestas en la guía, Participación en el grupo de WhatsApp de ciencias naturales. |
| calificable? | 0 |
| Activo | 1 |
Propósito
GUÍA # 2:
Que el estudiante comprenda el origen de los nombres de los elementos químicos y realice la búsqueda de propiedades como la electronegatividad en la tabla periódica .
Motivación
Observa y realiza la siguiente infografía en un papel de tamaño grande:

Explicación
1. ORIGEN DE LOS NOMBRES DE LOS ELEMENTOS QUÍMICOS:
Hg: mercurio: el origen lo encontramos en el nombre que le daba Dioscórides (medico de la antigua Grecia): plata acuática (en griego hydrárgyros: hydra = agua, gyros = plata).
C: carbono: cuyo origen se supone griego carbonis o latino carbón, o el S: azufre: latín sulphur.
U: uranio Np: neptunio y Pu: plutonio.
Te: telurio: nombre de la Tierra en latín
P: fósforo: nombre de Venus también en latín.
Se: Selenio: luna en griego
He: helio: sol en griego
Ce: Cerio y Pd: paladio: por Ceres y Palas, los primeros asteroides descritos.
Nombres derivados de la mitología:
Ta: tantalio, tántalo: hijo de Zeus.
Prometio: en honor a Prometeo, el personaje mitológico que robó el fuego a los dioses para la humanidad, el titanio procedente de los Titanes, hijos de Urano, el iridio diosa griega Iris, el torio en referencia a Thor, dios de la guerra nórdico] o el vanadio [deriva de la diosa de la belleza en la mitología nórdica.
Según el personaje histórico al que hace honor el nombre, se presentan los restantes elementos clasificados dentro de este grupo ordenados por número atómico creciente:
•Curio: Pierre y Marie Curie •Fermio: Enrico Fermi (Físico italiano, desarrolló el primer reactor nuclear) •Nobelio: Alfred Nobel •Rutherfordio: Ernest Rutherford •Bohrio: Niels Bohr •Roentgenio: Wilhelm Conrad Roent (ingeniero mecánico y físico alemán).
Nombre de los elementos según los compuestos que forman:
Hidrógeno: deriva de los términos griegos hydro y gen: generador de agua, oxígeno por su parte significa generador de ácidos, mientras que nitrógeno, generador de nitratos (Ej. HNO3).
Otras propiedades cuya importancia ha hecho que pasen a la historia dando nombre a los elementos que las poseen son por ejemplo el olor, en el osmio [del griego osme: olor, debido al fuerte olor del OsO4.
Bromo del griego bromos: hedor, peste
2. ELECTRONEGATIVIDAD DE LOS ELEMENTOS QUÍMICOS:
La electronegatividad es la capacidad de un átomo para atraer a los electrones, cuando forma un enlace químico en una molécula. Así aumenta la electronegatividad de los elementos químicos en la tabla periódica:
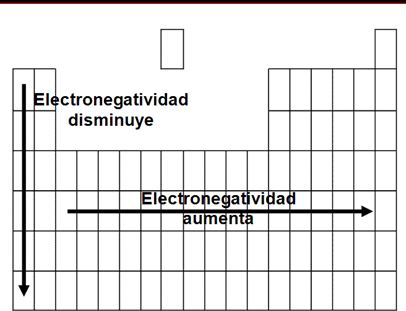
Ejercicios
1. Realizar en un papel de tamaño grande la infografía de la motivación.
2. Organiza en un esquema circular los elementos estudiados con su origen de nombre. ejemplo de esquema circular:

Evaluación
1. Ordenar de menor a mayor electronegatividad los siguientes elementos químicos, colocar el nombre del elemento y el tipo del elemento:
Cl, S, Sn, Pb, Na, K, Mg, Co, C, Ni, N, O, P, Fe, I, H, Ca, As, He, Ne, Ar, Rn, F, Br, At, Zn, Cu, La, Ba, Fr, Li.
NOTA: para realizar el ejercicio necesitas la tabla periodica.
Bibliografía
Foro
Cursos
| Curso | |
|---|---|
No results found. | |
Acceso a las actividades
| Actividad | Nombre | Fecha de ingreso | Fecha de actualización | Número de ingresos | Año | Curso | Subreporte |
|---|---|---|---|---|---|---|---|
No results found. | |||||||
