| Tema | Estados de agregación |
|---|---|
| Evidencia | |
| calificable? | 1 |
| Activo | 1 |
Propósito
Establece relaciones entre la teoría cinético-molecular y el estado en que se encuentra el material a través de gráficos, cuadro comparativos y resolución de problemas para predecir cambios físicos de acuerdo a las variables de estado.
Motivación
Ya en la antigua Grecia (siglos IV y V a. C.) los filósofos supusieron que la materia podía fraccionarse hasta obtener partículas muy pequeñas que llamaron átomos. Pensaban que estas partículas no podían dividirse más y que existía espacio vacío entre ellas (sin materia). Esto lo dedujeron a partir de experiencias de su vida cotidiana. Por ejemplo, sabían que el perfume de un ramo de flores ubicado en un sector de una habitación finalmente llegaba a lugares más alejados. Explicaron estos fenómenos suponiendo que todo está formado por partículas pequeñas que se mueven con cierta energía y se mezclan entre ellas. Nuestro planeta tiene elementos muy especiales, que lo hacen diferente a los demás planetas del Sistema Solar, como la presencia de la atmosfera. ¿Cuál es la importancia de la atmosfera?

Explicación
Las ideas acerca del movimiento de partículas en sólidos, líquidos y gases pueden resumirse en la teoría cinética de la materia.

La materia se presenta en cuatro estados de agregación: sólido, líquido, gas y plasma. Tan solo unas pocas sustancias se encuentran en la naturaleza en varios estados de agregación al mismo tiempo, como el caso del agua. El resto de las sustancias se encuentra en un estado concreto.
Cada uno de los estados de agregación tiene características definidas y, dependiendo de las condiciones externas como la presión y la temperatura, una misma sustancia puede pasar de un estado de agregación a otro. Estos cambios físicos tienen una característica particular y es que, mientras coexisten ambos estados, durante el cambio de estado la temperatura permanece constante.
Puedes apoyarte en esta presentación para profundizar en el tema (Estados de agregación)
Ejercicios
La presión atmosférica
UNA CIUDAD EN LAS ALTURAS
La Rinconada es la ciudad del mundo que se encuentra a mayor altitud; sus habitantes viven a 5100 metros sobre el nivel del mar.Ten en cuenta que los turistas que visitan La Rinconada pueden sufrir dificultades en la respiración, fatiga, mareos, dolores de cabeza, etc. Este conjunto de síntomas, relacionados con las condiciones atmosféricas en altura, se conoce como mal de altura.
Completa las frases siguientes.
a. Como la Rinconada se encuentra a menor / mayor altura que Los Ángeles, la masa de la columna de aire sobre la ciudad peruana es menor / mayor que en la ciudad norteamericana.
b. En la Rinconada las partículas de gas están más / menos compactadas que en Los Ángeles, de modo que la densidad del aire en la ciudad peruana es menor / mayor que en la ciudad norteamericana.
c. Diremos que la presión atmosférica en La Rinconada es menor / mayor que en Los Ángeles.
d. El aire ejerce fuerzas de más / menos intensidad sobre las superficies de los cuerpos en La Rinconada que en Los Ángeles.
Evaluación
En la capa de ozono
Lee el texto y responde las preguntas que se plantean:
La capa de ozono es un cinturón natural de gas ozono que se sitúa entre 15 y 30 kilómetros sobre la Tierra y actúa como un escudo ante la dañina radiación ultravioleta B (UVB) emitida por el sol.
El ozono es una molécula altamente reactiva formada por tres átomos de oxígeno. Sus moléculas se forman y se descomponen constantemente en la estratosfera, una región de la atmósfera superior situada entre los 10 y 50 km de altitud.
En la actualidad, hay una preocupación extendida acerca del deterioro de la capa de ozono causado por la liberación de contaminantes que contienen cloro. Dicho deterioro permite que grandes cantidades de rayos UVB, que pueden provocar cáncer de piel y cataratas en humanos y dañar a los animales, lleguen a la Tierra.
El exceso de radiación UVB también inhibe el ciclo reproductivo del fitoplancton, organismos unicelulares como las algas que componen el último eslabón de la cadena alimenticia. Los biólogos temen que una reducción de las poblaciones de fitoplancton provoque también reducciones de población en animales. Los investigadores también han documentado cambios en las tasas reproductivas de peces jóvenes, gambas y cangrejos, así como de ranas y salamandras cuando se exponen a un exceso de radiación UVB.
Los clorofluorocarbonos (CFC), sustancias químicas que se encuentran principalmente en los aerosoles en espray utilizados en los países industrializados durante los últimos 50 años, son los principales culpables del deterioro de la capa de ozono. Cuando los CFC alcanzan las capas altas de la atmosfera, se exponen a los rayos ultravioleta, lo que causa que liberen cloro entre otras sustancias. El cloro reacciona con los átomos de oxígeno del ozono y provoca la destrucción de sus moléculas.
Según la agencia para la protección del Medio Ambiente de EE. UU, un solo átomo de cloro puede destruir más de mil moléculas de ozono.
La capa de ozono sobre la Antártida ha sufrido un impacto considerable desde mediados de los años 80. Las bajas temperaturas de esta región aceleran la conversión de los CFC en cloro. En la primavera y el verano austral, cuando el sol brilla durante largos periodos del día, el cloro reacciona con los rayos ultravioleta y provoca la destrucción del ozono a gran escala, hasta el 65%. Esto es lo que algunas personas denominan erróneamente “agujero en la capa de ozono”. En otras regiones, la capa de ozono se ha deteriorado en un 20%.
Aproximadamente el 90% de los CFC que actualmente se encuentra en la atmósfera fueron emitidos por países industrializados del hemisferio norte, incluyendo los Estados Unidos y Europa: Estos países prohíben los CFC en 1996 y en la actualidad de cloro en la atmosfera está decreciendo. No obstante, los científicos calculan otros 50 años para que los niveles de cloro vuelvan a sus valores naturales.
1.- ¿Qué es la capa de ozono?
a. Una capa natural de la atmósfera capaz de absorber la radiación UV, nociva para los seres vivos.
b. La estratosfera, la capa superior de la atmósfera.
c. Una capa de gases contaminantes, producidos por la actividad humana, que se acumulan en la atmosfera y absorben radiaciones vitales para los seres vivos.
2.- ¿Qué son los CFC?
a. son abonos artificiales ricos en calcio utilizados en la jardinería.
b. Son complementos alimenticios para niños.
c. Una de capa de gases contaminantes, producidos por la actividad humana, que se acumulan en la atmosfera y absorben radiaciones vitales para los seres vivos.
3.- ¿Qué efecto provocan los CFC?
a. La creación de la capa de ozono
b. la destrucción de la capa de ozono
c. La destrucción de la estratosfera.
4.- ¿Cuáles de los átomos que forman el CFC son responsables de dicho efecto?
a. átomos de flúor
b. átomos de calcio
c. átomos cloro
d. átomos de carbono
d. átomos de fosforo
5.- ¿Cuál es la ecuación balanceada de la descomposición del ozono en oxígeno gaseoso?
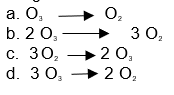
6.- ¿Cuál es el papel del cloro en la reacción?
a. Producto
b. Reactivo
c. Catalizador
7.- ¿Cuál de los componentes del contenido de una taza de café al que hemos añadido una cucharadita de azúcar es el disolvente?
a. ácidos
b. Cafeína
c. Azúcar
d. Otros componentes
e. Agua
8.- ¿Cuál de los componentes de un refresco carbonatado (con gas) es el disolvente?
a. Ácidos
b. Cafeína
c. Azúcar
d. Otros componentes
e. Agua
9.- ¿Qué propiedad o propiedades son características del disolvente de cualquier solución?
a. Es el componente soluble
b. Es el componente mayoritario
c. Es el componente líquido
10.- ¿Qué propiedad o propiedades son características de los solutos de cualquier solución?
a. Son componentes insolubles
b. Son componentes sólidos
c. Son componentes minoritarios
Acero inoxidable
Lee el texto con atención y contesta las preguntas que se plantean:
El acero inoxidable es tan común en nuestro día a día que casi todo el mundo ha tenido alguna vez en sus manos un artículo fabricado de este material. Pero ¿Cuántos de nosotros sabemos realmente lo que es el acero inoxidable?
Una clase de acero muy diferente
Como ocurre con todos los tipos de acero, el acero inoxidable no este compuesto por un único metal: es una aleación, una sustancia formada por dos o más componentes distintos que es mezclan o funden. Todos los aceros tienen en común que su principal componente metálico es el hierro, al que se añade una pequeña cantidad de carbono.
El acero inoxidable se invento a principios del siglo XX, cuando se descubrió que si se añadía una cierta cantidad de cromo al acero (mínimo un once por ciento), la mezcla adquiría un brillo satinado y se volvía muy resistente al desgaste y la oxidación. Precisamente la resistencia a la oxidación-también llamada resistencia a la corrosión-es la propiedad que distingue al acero inoxidable de los demás tipos de acero.
No es una capa
Es importante saber que el acero inoxidable es un material solido y no un revestimiento especial que se aplica al acero ordinario para darle propiedades “inoxidables”. Los aceros convencionales y, de hecho, muchos otros metales, suelen ser recubiertos o “chapados” con finas capas de metales blancos como el cromo, el níquel o el zinc con el fin de proteger o proporcionar otras características a sus superficies.
Aunque es cierto que los recubrimientos tienen sus ventajas y siguen siendo muy utilizados, también existe el riesgo de que estas finas capas sean perforadas o dañadas, lo que mina su efecto protector.
El acero inoxidable está en todas partes
Lógicamente el acero inoxidable debe su nombre a la resistencia que tiene a la oxidación. De todas formas, pronto se descubrió que este material presentaba muchas otras propiedades que lo hacían apropiado para una gran diversidad de usos. De hecho, el uso del acero inoxidable es casi ilimitado, como ilustran estos ejemplos:
- -En el hogar: cubertería, fregadero de la cocina, ollas y sartenes, hornos y barbacoas, etc.
- -En la ciudad: marquesinas del transporte público, mobiliario urbano, ascensores y escaleras mecánicas, trenes de metro e infraestructura de estaciones, etc.
- -En la industria: estructuras de plantas químicas y petroquímicas, componentes para motores de automoción y aeronáuticos, tanques químicos y de combustibles, etc.
“Introducción to Stainless Steel”, publicado en la página web del International Stainless Steel Fórum (ISSF):
11.-El acero inoxidable es…
a. Un metal
b. Una mezcla homogénea
c. Un compuesto
d. Una sustancia pura
e. Una aleación
f. Una solución
g, Una mezcla heterogénea
12.-En el acero inoxidable, el solvente es…
a. El carbono
b. El cromo
c. El hierro
13.- En el acero inoxidable, los principales solutos son…
a. El carbono
b. El cromo
c. El hierro
14.- ¿Qué diferencia al acero inoxidable del acero normal?
a. Su contenido en carbono
b. Su resistencia a la corrosión.
c. El recubrimiento que se aplica sobre el acero inoxidable.
d. La presencia de cromo
e. Nada; son dos formas distintas de llamare a la misma aleación.
f. La presencia de hierro
15.- Andrés tiene un gas en un recipiente cerrado, el cual tiene un émbolo que se puede mover hacia arriba o hacia abajo, como lo muestra la figura.
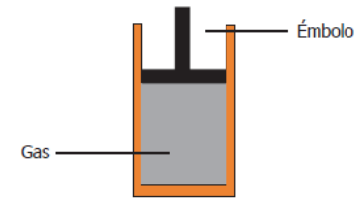
Andrés quiere que el volumen del gas aumente y que posteriormente disminuya. ¿Qué procesos deberá realizar Andrés sobre el gas para que esto ocurra?
A. Enfriar el gas y posteriormente halar el émbolo hacia arriba.
B. Poner una masa sobre el émbolo y posteriormente calentar el gas.
C. Poner una masa sobre el émbolo y posteriormente enfriar el gas.
D. Calentar el gas y posteriormente poner una masa sobre el émbolo.
Bibliografía
Hola química. Editorial Susaeta
Investiguemos 10. Editorial Voluntad
Química 10, Contextos Naturales. Editorial Santillana
Foro
Cursos
| Curso | |
|---|---|
No results found. | |
Acceso a las actividades
| Actividad | Nombre | Fecha de ingreso | Fecha de actualización | Número de ingresos | Año | Curso | Subreporte |
|---|---|---|---|---|---|---|---|
No results found. | |||||||
